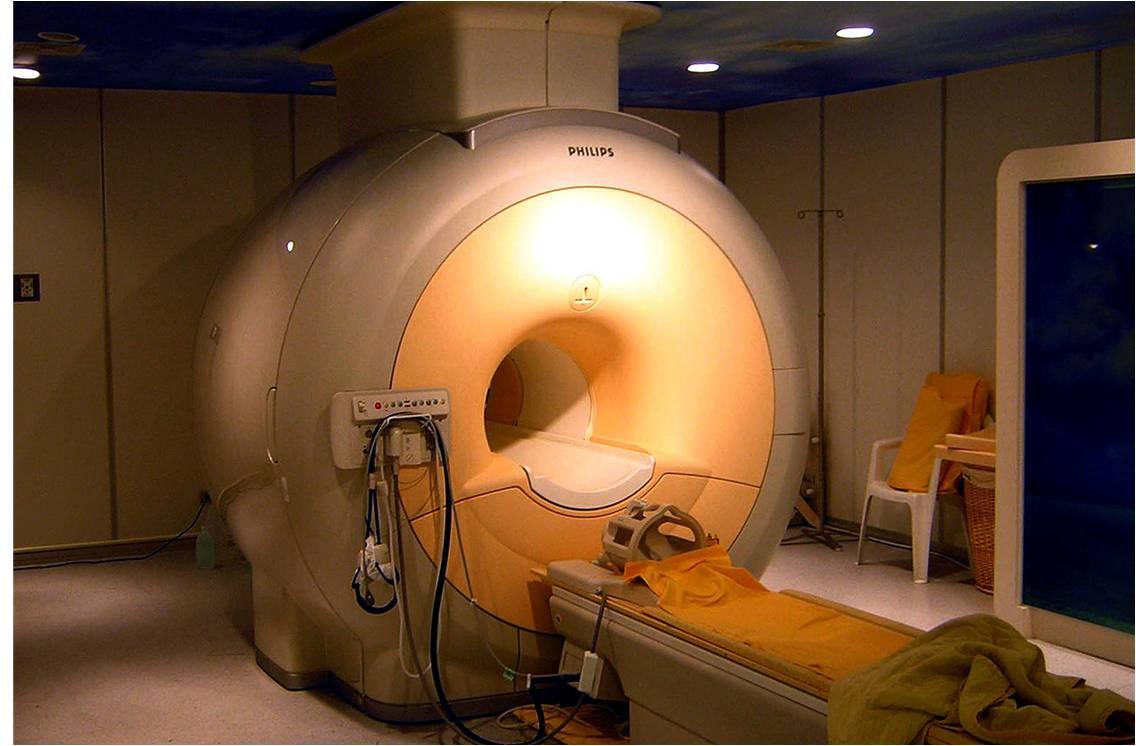
L'imagerie par résonance magnétique (IRM) est l'examen de référence pour explorer les tumeurs du système nerveux central (illustration @KasugaHuang sur Wikimedia).
La fin d'une rupture de stock qui durait depuis 2013
La spécialité BICNU 100 mg poudre et solvant pour solution pour perfusion (carmustine) est à nouveau disponible depuis le 21 janvier 2016.
BICNU était en rupture de stock depuis 2013 (notre article du 12 novembre 2013), en raison d'un problème de production puis d'un changement de laboratoire exploitant, précédemment le laboratoire Bristol-Myers Squibb.
Au cours de cette période d'indisponibilité, des spécialités équivalentes ont été importées afin de maintenir un approvisionnement en carmustine sur le marché français, notamment des unités de BICNU initialement destinées au marché américain.
Depuis septembre 2015, une spécialité initialement destinée au marché autrichien et équivalente à BICNU, CARMUBRIS, était ainsi mise à disposition en France (notre article du 11 septembre 2016).
Une remise à disposition pérenne selon le titulaire
Le laboratoire exploitant CSP (Centre Spécialités Pharmaceutiques) a confirmé avoir reçu un stock d'unités de BICNU suffisant pour répondre aux besoins du marché français.
Joint par téléphone, CSP précise que "le laboratoire titulaire de BICNU a annoncé être en mesure d'assurer un réapprovisionnement pérenne".
Des unités à réserver cependant aux seules indications de l'AMM
Seule spécialité de carmustine injectable disponible en France, BICNU a pour indication préférentielle le traitement des tumeurs du système nerveux central, conséquence de ses propriétés.
BICNU est utilisé seul ou en association dans le traitement des :
- tumeurs cérébrales primitives ou secondaires,
- myélomes multiples (Cf. VIDAL Reco Myélome multiple),
- lymphomes hodgkiniens,
- lymphomes non hodgkiniens (Cf. VIDAL Reco Lymphome non hodgkinien ganglionnaire de l'adulte),
- mélanomes (Cf. VIDAL Reco Mélanome cutané).
Le laboratoire CSP rappelle que les unités de BICNU remises à disposition doivent être réservées à ces seules indications validées par l'AMM en vigueur.
S'agissant du traitement du mycosis fongoïde, un médicament contenant de la chlorméthine, VALCHLOR gel, est disponible en France depuis le 14 novembre 2014 (notre article du 19 septembre 2014) sous le statut d'ATU (autorisation temporaire d'utilisation) nominative.
Pour aller plus loin
BICNU, poudre et solvant pour solution pour perfusion (carmustine) : Remise à disposition (ANSM, 27 janvier 2016)
Sur VIDAL.fr
BICNU (carmustine) : mise à disposition d'une spécialité équivalente pour pallier la rupture de stock (11 septembre 2015)
BICNU (carmustine) : mise à disposition d'un stock limité d'unités importées pour l'été (1er juillet 2015)
BICNU (carmustine) : rupture de stock de la spécialité importée (25 novembre 2014)
Prise en charge des lymphomes cutanés de type mycosis fongoïde : ATU nominative pour VALCHLOR gel (19 septembre 2014, actualisé le 14 novembre 2014)
BICNU (carmustine) : mise à disposition début février d'unités importées en quantité limitée (27 janvier 2014)
BICNU (carmustine) : rupture de stock de la spécialité importée (26 décembre 2013)
BICNU 100 mg poudre et solvant pour perfusion : rupture de stock et mise à disposition d'une spécialité importée (12 novembre 2013)
BICNU 100 mg poudre et solvant pour solution pour perfusion : distribution contingentée (19 septembre 2013)

 3 minutes
3 minutes Ajouter un commentaire
Ajouter un commentaire




Commentaires
Cliquez ici pour revenir à l'accueil.