
L'anxiété importante et la dépression sont des symptômes fréquemment associés à la survenue d'un cancer du sein (illustration).
La dépression et l'anxiété, deux troubles très fréquents en cas de cancer du sein
Le cancer du sein est le plus fréquent des cancers de la femme et est responsable, en France, d'environ 12 000 décès par an.
Selon plusieurs études observationnelles, près de la moitié des femmes atteintes par ce cancer seraient sujettes à de l'anxiété, une dépression ou les deux durant la première année suivant le diagnostic.Par ailleurs, la mise sous tamoxifène peut entraîner des effets secondaires qui peuvent également angoisser, déprimer…
Afin de lutter contre ces troubles, qui peuvent s'avérer péjoratifs pour la survie avec ce cancer, les professionnels ont recours aux moyens thérapeutiques usuels : psychothérapie de soutien, médicaments si besoin, dont des antidépresseurs.
Les antidépresseurs ISRS, puissants inhibiteurs de CYP2D6, l'enzyme qui active le cytochrome P450
Les antidépresseurs les plus prescrits de nos jours sont des inhibiteurs sélectifs de la recapture de la sérotonine (ISRS, ou SSRI en anglais).
Parmi ces ISRS, la fluoxétine (PROZAC et génériques) et la paroxétine (DEROXAT et génériques) peuvent inhiber la CYP2D6, qui est l'enzyme qui va activer le cytochrome P450.
Or le tamoxifène a besoin de cytochrome P450 pour devenir actif…
Le tamoxifène, inhibiteur compétitif de l'estradiol prescrit dans les cancers du sein hormonodépendants, est une prodrogue dont seuls les métabolites sont actifs.
Or pour activer ces métabolites, clefs de l'efficacité du tamoxifène (réduction d'un tiers des décès par cancer du sein hormono-dépendant et de 22 % les décès toutes causes, selon Davies et coll. - Lancet 2011), il faut du cytochrome P450, qui va couper la molécule de tamoxifène en 2 métabolites actifs.
Donc chez les femmes prenant de la fluoxétine ou de la paroxétine pour une anxiété et/ou une dépression, il y a un risque de baisse d'efficacité du tamoxifène, la CYP2D6 n'étant plus là pour activer le cytochrome P450, lui-même indispensable pour activer le tamoxifène…
Une possible baisse d'efficacité du tamoxifène… voire un effet péjoratif sur la mortalité ?
Cette baisse d'activité du tamoxifène pourrait réduire son efficacité, comme c'est d'ailleurs mentionné dans les mentions légales des produits concernés.
De plus, une étude observationnelle publiée en 2011 dans le BMJ a constaté davantage de décès (par cancer du sein et toutes causes) chez des femmes prenant paroxétine + tamoxifène par rapport à des femmes prenant du tamoxifène avec d'autres ISRS, mais cette augmentation n'a pas été retrouvée, étrangement, chez des femmes prenant fluoxétine + tamoxifène.
Il existe donc un flou (normalement, si cette association augmentait la mortalité, elle le ferait avec ces 2 ISRS et non un seul) que Macarius Donneyong et ses collaborateurs de Boston ont tenté de lever en analysant les données d'un échantillon plus large de femmes américaines atteintes d'un cancer du sein et sous ISRS, inhibiteurs de CYP2D6 ou non.
Comparaison des données de 14 500 femmes sous tamoxifène + ISRS, inhibant ou non l'enzyme CYP2D6
L'équipe de Joshua Gagne (Faculté Harvard, Boston) a donc comparé les données de deux cohortes constituées à partir des données de cinq assurances publiques et privées américaines :
- La première rassemblait les données de 6 067 femmes recevant pour la première fois du tamoxifène et qui se sont vu prescrire ultérieurement un ISRS.
- La deuxième rassemblait des données de 8 465 femmes déjà sous ISRS avant la prescription de tamoxifène.
Les caractéristiques individuelles étaient similaires dans les deux cohortes une fois les personnes appariées, avec un âge moyen de 56 et 55 ans respectivement.
Mortalité toutes causes comparable lorsque l'ISRS est initié avant ou après le démarrage du tamoxifène
La mortalité toutes causes dans un délai moyen de 2,2 ans a été de 64,3 / 1 000 personnes-année (991 décès sur 5 749 femmes) dans le premier groupe (initiation des ISRS après tamoxifène) et de 53,3 / 1 000 personnes-années (2 005 décès sur 13 542 femmes) dans le deuxième groupe (initiation des ISRS avant le tamoxifène).
Ces différences ne sont pas significatives sur le plan statistique, y compris lorsque les auteurs ont observé les résultats pour chaque base de données :
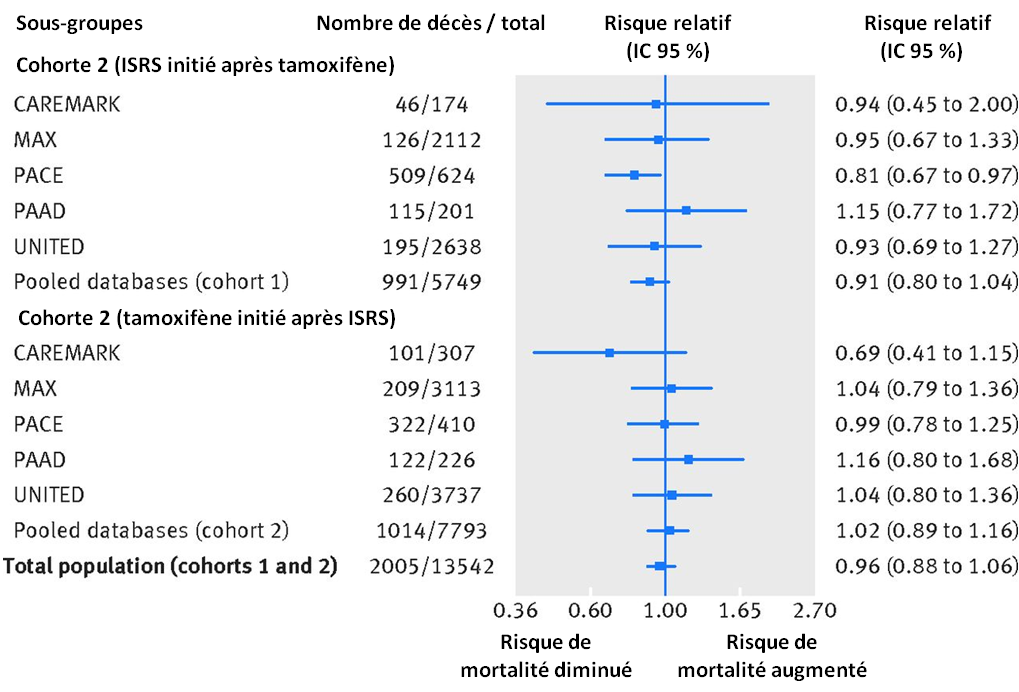
Mortalité toutes causes également comparable lorsque l'ISRS est ou n'est pas inhibiteur du CYP2D6
Dans le groupe poolé des femmes sous ISRS inhibiteurs du CYP2D6 (paroxétine ou fluoxétine), la mortalité était de 58,6 /1 000 personnes-années contre 57,9 /1 000 chez les femmes sous un autre ISRS, différence de risques non significative.
Pas d'influence non plus d'autres facteurs, excepté l'âge
Les auteurs ont ensuite analysé les résultats en fonction de la durée de prise de l'ISRS et du délai d'initiation du tamoxifène après le diagnostic, sans retrouver de différence significative de risques.
Par contre, la mortalité semble un peu plus élevée chez les femmes de moins de 51 ans sous ISRS (RR = 1,19 ; IC 95 % = 0,93 – 1,52) que chez les femmes de plus de 51 ans sous ISRS (RR = 0,93 ; IC 95 % = 0,84 – 1,03).
L'explication, à confirmer sur une plus longue durée et à explorer davantage, serait que le taux élevé d'estrogènes circulants des femmes en préménopause par rapport aux plus âgées rendrait l'inhibition compétitive du tamoxifène plus importante. Les auteurs souhaitent que des analyses poussées en sous-groupe éclaircissent cet éventuel effet de l'âge.
Plusieurs biais limitant la portée des conclusions positives de cette étude
Cette étude comporte plusieurs biais, notamment la jeunesse des femmes sélectionnées (54,7 ans d'âge moyen, contre 77 ans dans l'étude ayant levé un doute sur l'influence sur la mortalité de certainsISRS).
Autre biais relevé par les auteurs : le manque de détails ne permettant pas de distinguer la mortalité par cancer du sein dans leurs cohortes, ni de grader les cancers au moment de l'instauration du traitement par tamoxifène.
Enfin, le faible recul (2,4 ans de suivi en moyenne) ne permet pas d'exclure une éventuelle influence à moyen et long terme d'une prescription d'ISRS inhibiteurs (paroxétine ou fluoxétine) sur l'efficacité thérapeutique du tamoxifène.
Conclusion des auteurs : malgré ces limites, un impact insuffisant des ISRS inhibiteurs du CYP2D6 pour empêcher la métabolisation du tamoxifène, et donc son efficacité
Les auteurs soulignent que cette étude a permis de comparer le risque de mortalité chez des femmes prenant des ISRS inhibiteurs de CYP2D6 à celui de femmes sous ISRS non inhibiteurs, ce qui n'avait jamais été fait.
De plus, la séparation en deux cohortes avec une instauration de l'ISRS avant le tamoxifène (plutôt pour gérer l'anxiété et/ou la dépression) ou après (plutôt pour gérer l'impact psychologique des éventuels effets secondaires du tamoxifène) permet de vérifier l'absence d'impact des ISRS inhibiteurs dans deux situations différentes.
Enfin l'utilisation de plusieurs bases de données, incluant des femmes utilisant des assurances publiques ou privées, a permis d'élargir le champ des populations étudiées auparavant, ce qui fait espérer aux auteurs "une généralisation de leurs résultats à l'ensemble des Américaines" dans cette situation.
Les auteurs concluent donc, en s'appuyant sur les forces de leur étude, à l'absence d'effet sur la mortalité toutes causes d'une co-prescription tamoxifène et paroxétine/fluoxétine, cette absence d'effet ayant été constatée sur une large population de femmes sous ISRS, inhibiteurs de CYP2D6 ou non.
En savoir plus :
L'étude objet de cet article :
Macarius Donneyong, Katsiaryna Bykov, Pauline Bosco-Levy, et al. Risk of mortality with concomitant use of tamoxifen and selective serotonin reuptake inhibitors: multi-database cohort study. BMJ 2016;354:i5014
La méta-analyse sur l'efficacité du tamoxifène en cas de cancer du sein hormone-dépendant :
Davies C, Godwin J, Gray R, et al. Early Breast Cancer Trialists' Collaborative Group (EBCTCG). Relevance of breast cancer hormone receptors and other factors to the efficacy of adjuvant tamoxifen: patient-level meta-analysis of randomised trials. Lancet 2011;378:771- 84.
L'étude de cohort retrouvant un surrisque de mortalité avec la paroxétine, mais pas avec la floxétine
Kelly CM, Juurlink DN, Gomes T, et al. Selective serotonin reuptake inhibitors and breast cancer mortality in women receiving tamoxifen: a population based cohort study. BMJ 2010;340:c693.
Sources
Pour recevoir gratuitement toute l’actualité par mail Je m'abonne !

 6 minutes
6 minutes Ajouter un commentaire
Ajouter un commentaire





Commentaires
Cliquez ici pour revenir à l'accueil.