Classification pharmacothérapeutique VIDAL
Cancérologie - Hématologie > Antinéoplasiques > Modificateurs de la réponse immunitaire (BCG thérapie)
Urologie - Néphrologie > Tumeurs superficielles de vessie (BCG-thérapie)
Classification ATC
ANTINEOPLASIQUES ET IMMUNOMODULATEURS > IMMUNOSTIMULANTS > IMMUNOSTIMULANTS > AUTRES IMMUNOSTIMULANTS (VACCIN BCG)
Excipients
polygéline,
glucose anhydre,
polysorbate 80 excipient du solvant : sodium chlorure, eau ppi
Présentations
BCG-MEDAC Pdre/solv p susp intravésic Fl pdre+Poch/50ml+disp
Cip : 3400930018644
Modalités de conservation : Avant ouverture : 2° < t < 8° durant 24 mois (Conserver à l'abri de la lumière, Conserver au réfrigérateur, Conserver dans son emballage, Ne pas congeler)
BCG-MEDAC Pdre/solv p susp intravésic Fl pdre+Poch/50ml
Cip : 3400935395672
Modalités de conservation : Avant ouverture : 2° < t < 8° durant 24 mois (Conserver à l'abri de la lumière, Conserver au réfrigérateur, Conserver dans son emballage, Ne pas congeler)
| | par flacon * |
Bactéries BCG**
| 2 x 108 à 3 x 109 UV*** |
Excipients : Poudre : polygéline, glucose anhydre, polysorbate 80.
Solvant : chlorure de sodium, eau pour préparation injectable.
* Après reconstitution.
**
Bacille de Calmette-Guérin, provenant de
Mycobacterium bovis, germe RIVM dérivé du germe 1173-P2
***
Unités viables.
Traitement du carcinome urothélial non invasif de la vessie :
- Traitement curatif du carcinome in situ.
- Traitement prophylactique de la récidive du :
- carcinome urothélial limité à la muqueuse :
- pTa G1-G2 s'il s'agit d'une tumeur multifocale et/ou récidivante ;
- pTa G3.
- carcinome urothélial envahissant la lamina propria mais non la musculeuse de la vessie (pT1) ;
- carcinome in situ.
POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
BCG-medac ne doit pas être administré par voie sous-cutanée, intradermique, intramusculaire ou intraveineuse ou sous forme de vaccin.
-
Traitement des symptômes, signes ou syndromes :
-
Cf Effets indésirables.
-
Précautions relatives à la manipulation :
- BCG-medac ne doit pas être manipulé dans la même pièce et par le même personnel que celui qui prépare des médicaments cytotoxiques pour administration intraveineuse. BCG-medac ne doit pas être manipulé par une personne atteinte d'un déficit immunitaire connu. Le contact de BCG-medac avec la peau ou les muqueuses doit être évité. Une contamination peut entraîner une réaction d'hypersensibilité ou une infection de la région concernée.
-
Renversement accidentel de BCG-medac :
- En cas de renversement accidentel d'une suspension de BCG-medac, traiter avec un désinfectant possédant une activité démontrée contre les mycobactéries. Les éclaboussures sur la peau doivent être traitées avec un désinfectant approprié.
-
Recommandations d'hygiène générale pour le patient :
- Il est recommandé de se laver les mains et la région génitale après les mictions. Ceci est particulièrement important lors des premières mictions après l'instillation de BCG. En cas de contamination de lésions cutanées, il est recommandé d'utiliser un désinfectant approprié.
-
Tests à la tuberculine :
-
-
Intradermoréactions :
- Le traitement intravésical par BCG-medac peut induire une sensibilité à la tuberculine et compliquer l'interprétation ultérieure des tests intradermiques à la tuberculine réalisés pour diagnostiquer une infection mycobactérienne. Dans ce cas, la réactivité du patient à la tuberculine devrait être réalisée avant l'administration de BCG-medac.
-
-
Détection du bacille de Calmette-Guérin :
- Les médecins doivent garder à l'esprit que des résultats négatifs pour la présence du germe d'une culture de biopsie et des résultats d'analyse négatifs n'excluent pas une infection systémique au BCG. Dans plusieurs cas, les germes n'ont pas été détectés même si le patient présentait une infection systémique au BCG. Les méthodes disponibles (microscopie, PCR et/ou cultures et/ou une détection histologique compatible avec la tuberculose) ne sont pas fiables.
-
Infections/réactions systémiques sévères au BCG :
- Une instillation traumatique peut provoquer une septicémie due au BCG accompagnée éventuellement d'un choc septique et d'une situation engageant le pronostic vital. Pour les options de traitement, cf Effets indésirables.
- L'infection urinaire doit être exclue avant chaque instillation vésicale de BCG (une inflammation de la muqueuse vésicale peut augmenter le risque de dissémination hématogène du BCG). Si une infection urinaire est diagnostiquée pendant le traitement par BCG, le traitement doit être interrompu jusqu'à la normalisation des résultats d'analyse d'urine et la fin du traitement par antibiotique.
- Le risque d'infections systémiques sévères dues au BCG ainsi que la nécessité du traitement antituberculeux doit être envisagée avant l'instauration du traitement par BCG, en particulier chez les patients âgés (voir Patients âgés) et les patients atteints d'insuffisance hépatique.
- Des infections/réactions systémiques sévères au BCG ont été signalées dans moins de 5 % de la population étudiée. Pour les signes et symptômes, cf Effets indésirables.
- En cas de suspicion d'une infection systémique, un spécialiste des maladies infectieuses doit être consulté. Une infection au BCG peut être potentiellement fatale. Veuillez consulter la rubrique Effets indésirables.
- Contrairement aux infections systémiques, le syndrome de Reiter se présente comme une réaction à médiation principalement immunitaire qui n'est pas nécessairement provoquée par la dissémination du BCG, mais qui peut être également déclenchée par le BCG localisé uniquement dans les voies urinaires.
-
Fièvre ou hématurie macroscopique :
- Le traitement doit être reporté jusqu'à la disparition de la fièvre concomitante ou de l'hématurie macroscopique.
-
Faible capacité vésicale :
- Les patients dont la capacité vésicale est faible courent un risque accru de contracture de la vessie.
-
HLA-B27 :
- Chez les patients qui sont HLA-B27 positifs, la survenue d'une arthrite réactionnelle ou syndrome de Reiter est plus fréquente.
-
Réactivation d'une infection latente au BCG (y compris le retard de diagnostic) :
- Des cas isolés de persistance du BCG dans le corps pendant plusieurs années ont été rapportés. Ces infections latentes au BCG peuvent resurgir des années après l'infection initiale et peuvent notamment donner lieu à une pneumopathie granulomateuse, des abcès, des anévrismes infectés, une infection d'un implant, d'un greffon ou du tissu environnant.
-
Le patient doit être averti de la possibilité de réactivation tardive d'une infection latente par le BCG et informé de la conduite à tenir en cas d'apparition de symptômes tels que fièvre et perte de poids de cause inconnue.
- En cas de suspicion de réactivation d'une infection latente au BCG, un médecin spécialiste des maladies infectieuses doit être consulté.
-
Patients âgés :
- L'administration du BCG chez les patients âgés n'est pas contre-indiquée. Toutefois, le risque d'une infection/réaction systémique au BCG doit être envisagé avant de réaliser l'administration initiale. Les patients âgés peuvent souffrir d'insuffisance rénale ou hépatique, ce qui peut avoir une influence sur le traitement par des médicaments antituberculeux en cas d'infection/réaction systémique sévère au BCG. La prudence s'impose également pour les patients âgés présentant un état de santé affaibli.
-
Grossesse :
- BCG-medac n'est pas recommandé pendant la grossesse (cf Fertilité/Grossesse/Allaitement).
-
Patients en contact avec des personnes immunodéprimées :
- Les patients traités par BCG-medac doivent prendre des mesures hygiéniques adaptées s'ils sont en contact avec des patients immunodéprimés. M. bovis est moins pathogène que M. tuberculosis et aucune transmission de personne à personne n'a encore été signalée à ce jour, mais elle ne peut pas être exclue, en particulier chez les patients immunodéprimés.
-
Transmission sexuelle :
- Jusqu'à présent, une transmission sexuelle du BCG n'a pas été rapportée mais il est recommandé d'utiliser un préservatif pendant les rapports sexuels pendant une semaine après le traitement par BCG.
-
Traçabilité :
- Afin d'améliorer la traçabilité des médicaments biologiques, le nom et le numéro de lot du produit administré doivent être clairement enregistrés.
FERTILITÉ/GROSSESSE/ALLAITEMENT |
Grossesse :
Il n'existe pas de données ou il existe des données limitées sur l'utilisation du BCG chez la femme enceinte. Aucune étude sur la reproduction n'a été effectuée chez l'animal. BCG-medac n'est pas recommandé pendant la grossesse.
Allaitement :
Il n'existe pas de données suffisantes sur l'excrétion du BCG/métabolites dans le lait maternel. BCG-medac est contre-indiqué pendant l'allaitement (cf Contre-indications).
Fertilité :
Il a été observé que le traitement intravésical par BCG avait des effets nocifs sur la spermatogenèse et pouvait entraîner une oligospermie ou une azoospermie. Les études effectuées chez l'animal suggèrent que ces effets pourraient être transitoires et réversibles. Cependant, il est souhaitable que les hommes se fassent conseiller sur les possibilités de conservation du sperme avant de débuter le traitement.
CONDUITE et UTILISATION DE MACHINES |
Des symptômes locaux ou systémiques pendant un traitement par BCG-medac peuvent affecter l'aptitude à conduire des véhicules et à utiliser des machines.
Le surdosage est peu probable car un flacon de BCG-medac correspond à une dose.
Il n'existe pas de données indiquant qu'un surdosage peut provoquer d'autres symptômes que les effets indésirables décrits.
La toxicité, les propriétés d'immunostimulation et l'activité antitumorale de la souche RIVM du BCG ont été étudiées chez différents animaux. Des doses élevées de BCG ont provoqué un retard pondéral chez la souris et des troubles hépatiques ont également été observés. L'injection intraveineuse chez le lapin semblait être pyrogène. Des instillations répétées chez le cobaye ont induit des réactions inflammatoires dans la paroi vésicale. Des effets indésirables comme des lésions granulomateuses du foie et des poumons sont survenues aux doses élevées. L'administration intravésicale chez le chien indiquait des petites lésions mécaniques de l'urothélium alors qu'aucun signe d'inflammation active n'a été observé dans le stroma sous-urothélial.
Aucune étude sur la mutagenèse, la carcinogenèse et la reproduction n'a été faite.
BCG-medac ne doit pas être mélangé avec les solutions hypotoniques et hypertoniques.
MODALITÉS DE CONSERVATION |
Durée de conservation : 2 ans ou 3 ans si le nombre des unités vivantes lors de la libération est plus grand que 5 x 108 CFU/flacon, en tout cas pas au-delà de 4 ans à partir de la date de récolte.
A conserver au réfrigérateur (entre 2 °C et 8 °C).
Ne pas congeler.
A conserver dans l'emballage d'origine, à l'abri de la lumière.
Après reconstitution, le produit doit être utilisé immédiatement.
MODALITÉS MANIPULATION/ÉLIMINATION |
-
Instructions pour l'utilisation/la manipulation :
- La mise en place du cathéter doit être réalisée avec précaution afin d'éviter des lésions de l'épithélium qui pourraient entraîner l'apparition d'une infection systémique par le BCG. L'utilisation d'un lubrifiant est recommandée afin de limiter au maximum le risque de cathétérisme traumatique et de réduire l'inconfort du patient. La quantité de lubrifiant nécessaire peut être moins importante chez les femmes que chez les hommes. Le drainage de la vessie après le cathétérisme permet de réduire les résidus de lubrifiant avant d'appliquer le BCG.
- Avant utilisation, le produit doit être remis en suspension dans des conditions d'asepsie avec une solution de chlorure de sodium à 0,9 % stérile (voir ci-dessous). Mélanger à nouveau la suspension avant son utilisation en faisant délicatement tourner le flacon. Éviter le contact de BCG-medac avec la peau. Le port de gants est recommandé.
- La présence de particules macroscopiques visibles n'affecte pas l'efficacité ni la sécurité d'emploi du médicament.
- Pour de plus amples informations sur le cathéter, veuillez consulter le mode d'emploi correspondant.
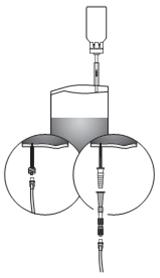
- Les instructions de manipulation ci-dessous concernent le système avec adaptateur Luer-Lock.
-
-
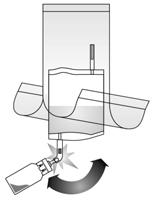
- Déchirer la poche de protection mais ne pas la retirer complètement ! Ceci empêchera la contamination de l'extrémité du système d'instillation jusqu'à la dernière minute.
- Enlever les opercules du flacon et du système d'instillation. Préparer un sac pour l'élimination de déchets.
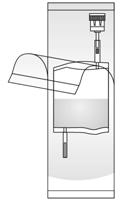
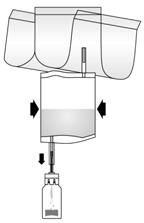
- Poser le flacon de BCG-MEDAC sur une surface solide (par ex. une table) et bien enfoncer l'adaptateur pour flacon du système d'instillation à la verticale sur le flacon de BCG-MEDAC. Faire tourner le flacon 2 fois complètement dans le même sens
- Rompre le mécanisme dans le tube de l'adaptateur pour flacon en le courbant plusieurs fois vers l'avant et vers l'arrière. Ceci établit la connexion. Tenir le tube - et non le flacon - pendant ce processus !
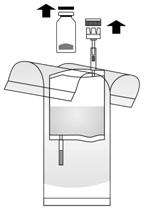
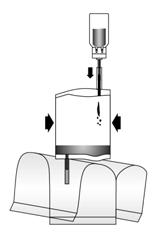
- Pomper le liquide dans le flacon, mais ne pas remplir le flacon complètement. Si l'écoulement ne se fait pas, tourner à nouveau le flacon 2 fois complètement dans le même sens pour assurer que le septum est complètement transpercé. Répéter cette étape jusqu'à ce que le liquide s'écoule.
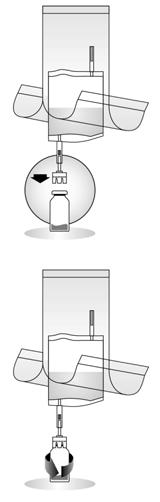
- Renverser l'ensemble du système. Pomper de l'air à partir du système d'instillation jusque dans le flacon situé au-dessus et faire passer le BCG-medac reconstitué dans le système d'instillation. Ne pas retirer le flacon.
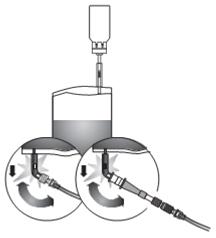
- Maintenir le système d'instillation en position verticale. Puis, retirer complètement la poche de protection. Connecter le cathéter (et un adaptateur [conique en Luer-Lock]) au système d'instillation. Rompre le mécanisme de fermeture dans le tube en le courbant en faisant des allers-retours et instiller la suspension de BCG-medac. A la fin de l'instillation, désobstruer le cathéter en y faisant passer de l'air. Continuer à comprimer le système d'instillation et le placer avec le cathéter dans le sac à déchets.
- Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
LISTE I
| Prescription initiale hospitalière 6 mois et renouvellement réservés aux spécialistes en urologie ou en oncologie médicale. |
| AMM | 3400930018644 (2002, RCP rév 29.01.2024). |
| | |
| Prix : | 157,15 euros (boîte de 1 + cathéter). |
| Remb Séc soc à 100 %. Collect. |
Titulaire de l'AMM : Medac, Gesellschaft für Klinische, Spezialpräparate mbH, Theaterstr. 6, 22880 Wedel, Allemagne.