Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- FIBROVEIN
- FIBROVEIN 3 % sol inj
Mise à jour : 18 septembre 2024
Sommaire
SYNTHÈSE |
EEN sans dose seuil : alcool benzylique
Cip : 3400926883607
Modalités de conservation : Avant ouverture : durant 36 mois (Conserver à l'abri de la lumière, Conserver dans son emballage, Ne pas congeler)
FORMES et PRÉSENTATIONS |
Solution injectable (limpide, incolore et stérile, sans particules visibles ; de pH : 7,5-7,9 et d'osmolarité : 247-273 mOsmol/kg).
Ampoule contenant 2 mL de solution. Boîte de 5.
COMPOSITION |
Pour 1 mL de solution injectable :
Tétradécyl sulfate de sodium : 30 mg
Chaque ampoule de 2 mL contient 60 mg de tétradécyl sulfate de sodium.
Excipient(s) à effet notoire :
Ce médicament contient 20 mg d'alcool benzylique par mL de solution injectable.
Ce médicament contient approximativement jusqu'à 3,1 mg de sodium par mL de solution injectable, c'est-à-dire qu'il est essentiellement « sans sodium ».
Ce médicament contient 0,3 mg de potassium par mL de solution injectable, c'est-à-dire qu'il est essentiellement « sans potassium ».
Alcool benzylique, phosphate disodique dodécahydraté, dihydrogénophosphate de potassium, hydroxyde de sodium (pour ajustement du pH), eau pour préparations injectables.
INDICATIONS |
FIBROVEIN est réservé à l'adulte.
Traitement des varices primaires non compliquées, des varices récidivantes ou résiduelles suite à une intervention chirurgicale, des veines réticulaires, des veinules et des varicosités des membres inférieurs caractérisées par une dilatation simple.
POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Précautions générales
L'utilisation de FIBROVEIN doit être réservée aux médecins ; lorsque la réglementation nationale l'autorise, FIBROVEIN peut être administré sous la surveillance d'un médecin par un professionnel de santé ayant les qualifications appropriées, expérimenté en anatomie veineuse, diagnostic et traitement des pathologies affectant le système veineux et préalablement formé à la technique d'injection.
Des réactions allergiques (notamment des réactions anaphylactiques) ayant été observées, le médecin doit être préparé à la survenue possible d'une réaction anaphylactique et doit être prêt à la traiter convenablement. Le matériel de réanimation d'urgence doit être immédiatement disponible.
Avant le traitement, le médecin ou le professionnel de santé ayant les qualifications appropriées qui administre FIBROVEIN sous la surveillance d'un médecin doit rechercher les facteurs de risque et informer le patient des risques que présente la technique envisagée.
La sclérothérapie est contre-indiquée chez les patients présentant un risque élevé d'événements thromboemboliques, mais doit être évitée dans la plupart des situations à moindre risque. Elle n'est notamment pas recommandée chez les patients ayant des antécédents d'événements thromboemboliques. Néanmoins, si la sclérothérapie est jugée nécessaire, une thérapie d'anticoagulation préventive peut être initiée.
Foramen ovale perméable (FOP)
En raison de la circulation possible de produit, de bulles ou de particules dans la partie droite de cœur, la présence d'un FOP peut favoriser la survenue de graves effets artériels indésirables. Il est recommandé d'effectuer la recherche d'un FOP avant de débuter la sclérothérapie chez les patients ayant des antécédents de migraine avec aura, d'accidents cérébro-vasculaires graves, ou d'HTAP.
Chez les patients atteints de FOP connu, mais asymptomatique, il est recommandé d'utiliser des volumes plus faibles et d'éviter tout effort à glotte fermée (manœuvre de Valsalva) pendant les minutes qui suivent l'injection.
Les patients atteints d'un FOP se sont avérés être plus susceptibles de souffrir d'effets indésirables tels que des incidents neurologiques temporaires, des affections oculaires et des migraines. Un FOP symptomatique est une contre-indication pour l'usage de FIBROVEIN en mousse (voir rubrique Contre-indications).
Migraine
Les patients ayant des antécédents de migraine doivent être traités avec précaution. Les patients migraineux se sont avérés être plus susceptibles de souffrir d'affections oculaires et de migraine, en particulier après les injections de mousse sclérosante.
Utiliser des volumes plus faibles chez les patients ayant des antécédents de migraine.
Accident ischémique transitoire (AIT)
Les patients ayant des antécédents d'AIT doivent être traités avec précaution.
Ces patients se sont avérés plus susceptibles de souffrir de troubles visuels et de migraine, en particulier après les injections de mousse sclérosante.
Varices tronculaires
Lors du traitement de varices tronculaires, l'injection de mousse doit être effectuée à une distance minimale de 8 à 10 cm par rapport à la jonction saphéno-fémorale.
Lymphœdème
Si l'insuffisance veineuse est associée à un lymphœdème, l'injection sclérosante peut aggraver la douleur et l'inflammation locales pendant plusieurs jours ou plusieurs semaines. Les patients doivent être informés de l'éventualité de cette phase, ce qui ne compromet en aucun cas l'efficacité.
Extravasation
De graves effets indésirables au niveau local, incluant la nécrose tissulaire, peuvent se produire suite à une extravasation. Par conséquent, faire preuve d'une grande prudence lors du positionnement de l'aiguille par voie intraveineuse et utiliser le volume minimal efficace à chaque site d'injection. Une pigmentation peut être favorisée en cas d'épanchement sanguin au niveau du site d'injection (en particulier lors du traitement des veines superficielles de petit calibre) et quand la compression n'est pas utilisée.
Injection intra-artérielle
Ne jamais injecter les sclérosants dans une artère, car cela pourrait provoquer une nécrose tissulaire et conduire à l'amputation. Pour éviter des extravasations et une injection artérielle, il est recommandé d'effectuer l'injection sous échographie duplex.
Le patient doit être surveillé pendant et après l'administration de FIBROVEIN. Des manifestations d'hypersensibilité (rougeur, prurit, toux) ou des manifestations neurologiques (scotomes, amaurose, migraine avec aura, paresthésie, déficit focalisé) peuvent se produire.
Affections respiratoires
Une attention particulière doit être portée aux patients présentant une respiration difficile (asthme bronchique) ou une forte prédisposition aux allergies (voir rubrique Posologie et mode d'administration).
Évaluation pré-injection
En raison du risque d'extension de thrombose dans le système veineux profond, il est indispensable d'évaluer soigneusement la continence valvulaire avant toute injection et d'injecter lentement de faibles quantités de produit dans la varice (pas plus de 2 mL). La perméabilité des veines profondes doit être évaluée par une méthode non invasive telle que l'échographie duplex. La sclérothérapie veineuse ne doit pas être réalisée si une incontinence valvulaire significative ou une insuffisance veineuse profonde est détectée, lors des épreuves de Trendelenburg ou de Perthes, ou lors d'une phlébographie par exemple.
Surveillance post-injection
Il est recommandé de réaliser un examen de suivi clinique et échographique à environ 1 mois, afin de contrôler l'efficacité du traitement et la survenue d'éventuels effets indésirables. En effet, des cas de thrombose veineuse profonde et d'embolie pulmonaire ont été rapportés après sclérothérapie de varices superficielles, jusqu'à 4 semaines après l'injection de tétradécyl sodium sulfate. La mise en place d'une compression adaptée après le traitement peut également être envisagée pour réduire le risque de thrombose veineuse profonde.
Affections artérielles sous-jacentes
Une extrême prudence est recommandée en cas d'utilisation chez les patients atteints d'affections artérielles sous-jacentes, notamment en cas d'athérosclérose périphérique sévère ou de thromboangéite oblitérante (maladie de Buerger).
Pied et zone malléolaire
Une extrême prudence est recommandée en cas d'injection au niveau du pied et de la zone malléolaire du fait du risque accru d'injection accidentelle intra-artérielle.
Excipients
Ce médicament contient moins de 1 mmol de sodium (23 mg) par ampoule, c'est-à-dire qu'il est essentiellement « sans sodium ».
Ce médicament contient moins de 1 mmol de potassium (39 mg) par ampoule, c'est-à-dire qu'il est essentiellement « sans potassium ».
Ce médicament contient 40 mg d'alcool benzylique par ampoule de 2 mL, équivalent à 20 mg/mL. L'alcool benzylique peut provoquer des réactions allergiques. Demandez l'avis de votre médecin ou de votre pharmacien si vous êtes enceinte ou si vous allaitez, ou si vous souffrez d'une maladie du foie ou du rein. De grandes quantités d'alcool benzylique peuvent s'accumuler dans votre corps et entraîner des effets secondaires (appelés « acidose métabolique »).
INTERACTIONS |
Connectez-vous pour accéder à ce contenu
FERTILITÉ/GROSSESSE/ALLAITEMENT |
Grossesse
La sécurité d'emploi au cours de la grossesse n'est pas établie. A ce jour, il n'existe pas ou peu de données sur l'administration du tétradécyl sulfate de sodium chez la femme enceinte. Les études animales de reprotoxicité sont insuffisantes. Le traitement ne peut être initié qu'après la grossesse.
FIBROVEIN ne doit être utilisé qu'en cas de nécessité, pour le soulagement symptomatique, si les bénéfices potentiels l'emportent sur les risques potentiels pour le fœtus.
Allaitement
On ne sait pas si le tétradécyl sulfate de sodium est excrété dans le lait maternel. La prudence est recommandée lorsqu'il est administré chez les femmes qui allaitent.
Fertilité
On ne sait pas si le tétradécyl sulfate de sodium affecte la fertilité.
CONDUITE et UTILISATION DE MACHINES |
FIBROVEIN n'a aucun effet ou un effet négligeable sur l'aptitude à conduire des véhicules et à utiliser des machines. Cependant, l'utilisation d'un bandage et/ou de bas de contention peuvent s'avérer nécessaire après le traitement. Ceci peut affecter l'aptitude à conduire.
EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
SURDOSAGE |
Aucun cas de surdosage systémique n'a été rapporté. L'utilisation d'une concentration plus élevée que celle recommandée dans les petites veines peut conduire à une pigmentation et/ou une nécrose tissulaire locale.
PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
PHARMACOCINÉTIQUE |
Connectez-vous pour accéder à ce contenu
SÉCURITÉ PRÉCLINIQUE |
Il n'y a pas d'informations supplémentaires pour le prescripteur autres que celles déjà mentionnées dans d'autres sections du RCP.
INCOMPATIBILITÉS |
Ce médicament n'est pas compatible avec l'héparine.
En l'absence d'études de comptabilité, ce médicament ne doit pas être mélangé avec d'autres médicaments.
DURÉE DE CONSERVATION |
3 ans.
Après première ouverture, le médicament doit être utilisé immédiatement.
PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
Ce médicament ne nécessite pas de précautions particulières de conservation concernant la température.
Ne pas congeler.
Conserver l'ampoule dans l'emballage extérieur, à l'abri de la lumière.
PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
La mousse doit être préparée de manière extemporanée par un praticien préalablement formé à cette technique particulière de préparation et d'administration.
La préparation de la mousse doit se faire dans des conditions d'asepsie strictes.
Recommandations générales
La qualité de la mousse dépend de critères spécifiques :
Préparation de la mousse (technique Tessari) :
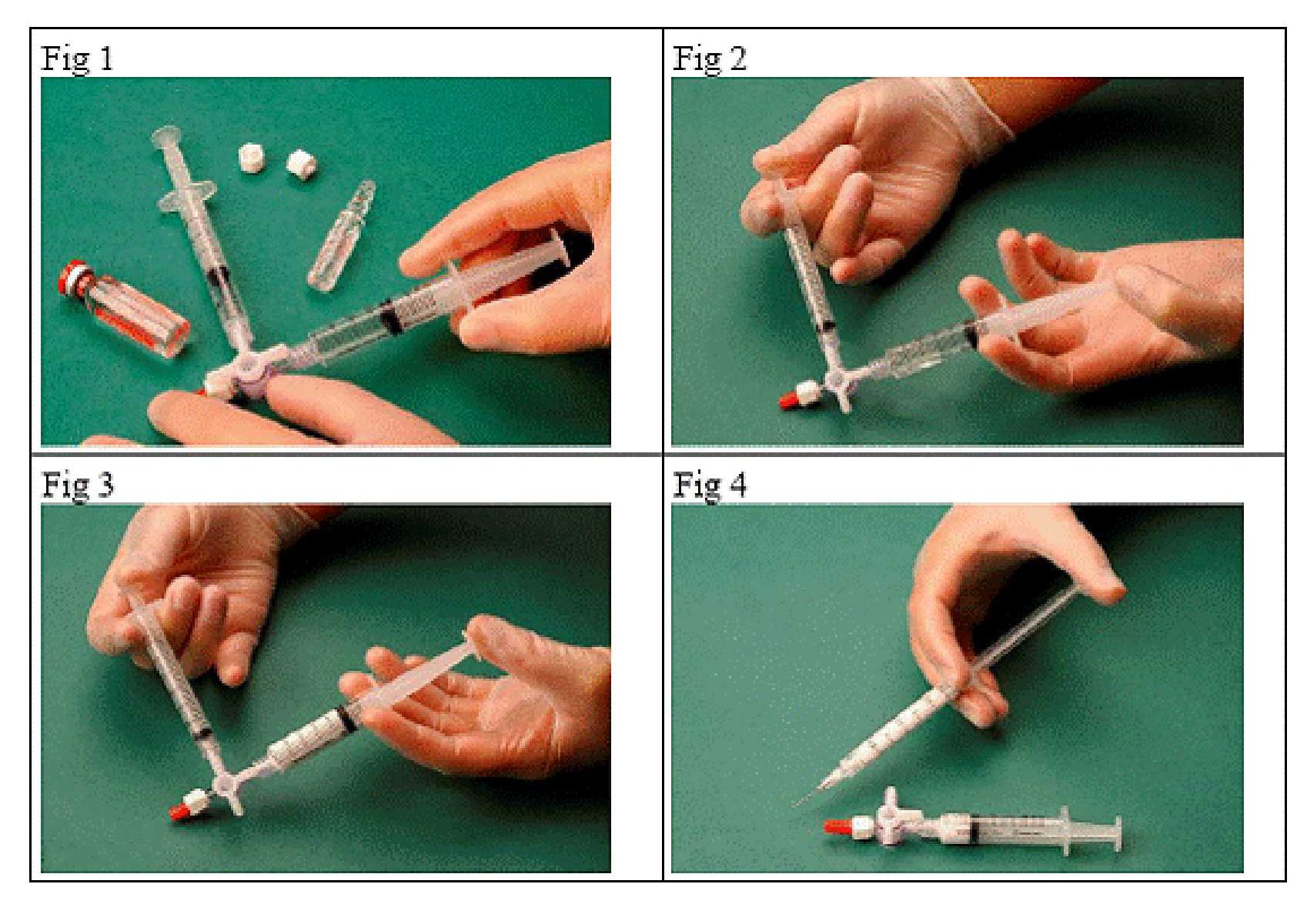
Pour préparer une mousse sclérosante, aspirer 1 mL de liquide sclérosant dans une seringue stérile et 3 mL ou 4 mL d'air stérile dans une autre seringue stérile. L'air est aspiré à travers un filtre de 0,2 μm afin d'assurer sa stérilité. Les seringues sont ensuite reliées en utilisant un système stérile de connexion à trois voies (Fig. 1). Il est conseillé d'utiliser des seringues Luer Lock et de porter des lunettes de protection lors de la préparation de la mousse. La pression peut provoquer la défaillance du système de connexion à trois voies avec les seringues Luer Slip et le produit peut jaillir de manière incontrôlée.
Le mélange sclérosant/air est alors passé d'une seringue à l'autre à travers le système de connexion à trois voies, au moins 20 fois, pour produire une mousse lisse et de bonne densité (Fig. 2 et 3).
La seringue contenant la mousse est ensuite retirée du système de connexion et la mousse est immédiatement injectée dans la veine (Fig. 4).
La mousse sclérosante doit être utilisée dans les soixante secondes qui suivent la préparation. Après soixante secondes, la mousse résiduelle doit être jetée. Il faut repréparer de la mousse si nécessaire.
La qualité de la mousse doit être vérifiée avant son administration. Elle doit avoir un aspect homogène, être de couleur blanche, sans grosses bulles visibles à l'œil nu.
Elimination
Tout médicament non utilisé ou déchet doit être éliminé conformément à la réglementation en vigueur.
PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|