Veuillez saisir au moins 3 caractères pour votre recherche.
- Médicaments
- LASILIX
- LASILIX 10 mg/ml sol buv
Mise à jour : 22 août 2024
Sommaire
SYNTHÈSE |
aromatisant : orange arôme, alpha-pinène, bêta-pinène, myrcène, limonène, octanal, décanal, linalol
EEN sans dose seuil : sorbitol, p-hydroxybenzoate de méthyle, p-hydroxybenzoate de propyle, jaune orangé S, éthanol à 96 %
Cip : 3400933000912
Modalités de conservation : Avant ouverture : < 30° durant 18 mois (Conserver à l'abri de la lumière, Conserver dans son emballage, Conserver à l'abri de l'humidité)
Après ouverture : < 30° durant 6 semaines (Conserver à l'abri de la lumière, Conserver dans son emballage, Conserver à l'abri de l'humidité)
FORMES et PRÉSENTATIONS |
Solution buvable.
Flacon de 60 ml, avec pipette doseuse.
COMPOSITION |
Pour un flacon de 60 ml :
Furosémide : 0,600 g
1 graduation de la pipette doseuse correspond à 0,1 ml de solution soit 1 mg de furosémide.
Excipients à effet notoire : Jaune orangé S (E110), éthanol 100,9 mg/ml, parahydroxybenzoate, sorbitol.
Sorbitol, glycérol, parahydroxybenzoate de méthyle, parahydroxybenzoate de propyle, arôme orange (alpha-pinène, bêta-pinène, myrcène, limonène, octanal, décanal, linalol, éthanol), jaune orangé S (E110), éthanol à 96 pour cent, hydroxyde de sodium, eau purifiée.
INDICATIONS |
POSOLOGIE ET MODE D'ADMINISTRATION |
Connectez-vous pour accéder à ce contenu
CONTRE-INDICATIONS |
Connectez-vous pour accéder à ce contenu
MISES EN GARDE et PRÉCAUTIONS D'EMPLOI |
Mises en garde spéciales
Avec le lithium, l'association est déconseillée (voir rubrique Interactions).
La prise accidentelle de furosémide peut entraîner une hypovolémie avec déshydratation (voir rubrique Surdosage).
Chez l'insuffisant hépatocellulaire, le traitement sera conduit avec prudence sous surveillance hydroélectrolytique stricte, compte tenu d'un risque d'encéphalopathie hépatique (cf. Précautions d'emploi). L'interruption du traitement devra alors être immédiate.
La prise de furosémide en cas d'obstruction partielle des voies urinaires peut exposer les patients à une rétention urinaire. Une surveillance étroite de la diurèse devra donc être instaurée, particulièrement en début de traitement par le furosémide.
Le furosémide est un sulfamide. La possibilité d'une allergie croisée avec les autres sulfamides, notamment antibactériens, reste théorique et non validée en clinique.
Des cas de réactions de photosensibilité ont été rapportés avec le furosémide (voir rubrique Effets indésirables).
En cas de survenue de réactions de photosensibilité sous traitement, il est recommandé d'interrompre le traitement. Si une réadministration du traitement est indispensable, il est recommandé de protéger les zones exposées au soleil ou aux UVA artificiels.
Excipients à effet notoire :
Ce médicament contient du sorbitol. Son utilisation est déconseillée chez les patients présentant une intolérance au fructose (maladie héréditaire rare).
Ce médicament contient du « parahydroxybenzoate » et peut provoquer des réactions allergiques (éventuellement retardées).
Ce médicament contient un agent colorant azoïque (E110 : jaune orangé S) et peut provoquer des réactions allergiques.
Ce médicament contient 100,9 mg d'éthanol par ml de solution buvable, équivalent à 10,09 % p/v. La quantité d'éthanol par ml de ce médicament est équivalente à 2,5 ml de bière ou 1 ml de vin.
La quantité d'éthanol contenue dans ce médicament n'est pas susceptible d'avoir un effet chez les adultes et les adolescents, et est peu susceptible d'avoir un effet notable chez les enfants. Chez les jeunes enfants, certains effets peuvent survenir comme par exemple la somnolence.
L'éthanol contenu dans ce médicament peut modifier les effets d'autres médicaments (voir rubrique Interactions).
Il doit être pris en compte chez les personnes souffrant d'alcoolisme, chez les femmes enceintes ou qui allaitent, et chez les enfants.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par prise, c'est-à-dire qu'il est essentiellement « sans sodium ».
Précautions d'emploi
Le traitement par le furosémide nécessite une surveillance particulière et une adaptation de la posologie pour les patients présentant un(e) :
Une hypotension symptomatique causant vertiges, évanouissements ou pertes de conscience peut apparaître chez certains patients traités par du furosémide, en particulier chez les patients âgés, les patients prenant d'autres traitements susceptibles de causer de l'hypotension et chez les patients présentant d'autres problèmes médicaux impliquant un risque d'hypotension.
Equilibre hydroélectrolytique :
Elle doit être contrôlée avant la mise en route du traitement, puis à intervalles réguliers par la suite. Tout traitement diurétique peut en effet provoquer une hyponatrémie, aux conséquences parfois graves.
La baisse de la natrémie pouvant être initialement asymptomatique, un contrôle régulier est donc indispensable et doit être encore plus fréquent dans les populations à risque représentées par les sujets âgés, a fortiori dénutris, et les cirrhotiques (voir rubriques Effets indésirables et Surdosage).
La déplétion potassique avec hypokaliémie constitue le risque majeur des diurétiques de l'anse. Le risque de survenue d'une hypokaliémie (< 3,5 mmol/l) doit être prévenu dans certaines populations à risques représentées par les sujets âgés et/ou dénutris et/ou polymédiqués, les cirrhotiques avec œdèmes et ascite, les coronariens, les insuffisants cardiaques. L'hypokaliémie majore la toxicité cardiaque des digitaliques et le risque de troubles du rythme. Chez les patients présentant un espace QT long à l'ECG d'origine congénitale ou médicamenteuse, l'hypokaliémie favorise la survenue de troubles du rythme sévères, en particulier des torsades de pointes, potentiellement fatales, surtout en présence d'une bradycardie. Dans tous les cas, des contrôles plus fréquents de la kaliémie sont nécessaires. Le premier contrôle du potassium plasmatique doit être effectué au cours de la semaine qui suit la mise en route du traitement.
Glycémie
L'effet hyperglycémiant est modeste. Le contrôle de la glycémie sera renforcé chez le diabétique et le pré-diabétique.
Uricémie
La déplétion hydrosodée induite par le furosémide réduit l'élimination urinaire d'acide urique. Chez les patients hyperuricémiques, la tendance aux accès de goutte peut être augmentée. Il conviendra d'être prudent chez le goutteux.
Créatininémie
Le contrôle régulier de la créatininémie est généralement recommandé durant le traitement par le furosémide.
Surveillance étroite des patients présentant des risques de troubles hydroélectrolytiques importants (vomissements, diarrhées, hypersudation...). Une déshydratation, une hypovolémie ou un déséquilibre acido-basique nécessitent un traitement correctif et peuvent conduire à interrompre temporairement le traitement.
Utilisation concomitante avec la rispéridone :
Dans les essais contrôlés versus placebo réalisés avec la rispéridone chez des patients âgés déments, une incidence plus élevée de la mortalité a été observée chez les patients traités par furosémide plus rispéridone (7,3 % ; âge moyen 89 ans, extrêmes 75-97 ans) comparativement aux patients traités par la rispéridone seule (3,1 % ; âge moyen 84 ans, extrêmes 70-96 ans) ou le furosémide seul (4,1 % ; âge moyen 80 ans, extrêmes 67-90 ans).
L'utilisation concomitante de rispéridone avec d'autres diurétiques (principalement des diurétiques thiazidiques administrés à faible dose) n'a pas été associée à des observations similaires.
Aucun mécanisme physiopathologique n'a été identifié pour expliquer cet effet, et aucun motif cohérent de décès n'a été observé.
Toutefois, la prudence est nécessaire et le rapport bénéfice/risque de cette association ou d'un traitement concomitant par d'autres diurétiques puissants doit être pris en compte préalablement à toute décision d'utilisation.
Il n'a pas été observé d'augmentation de la mortalité chez les patients prenant d'autres diurétiques comme traitement concomitant à la rispéridone. Indépendamment du traitement, la déshydratation est un facteur de risque de mortalité et doit donc être soigneusement évitée chez les patients âgés déments (voir rubrique Contre-indications).
L'exacerbation ou l'activation d'un lupus érythémateux disséminé est possible.
Sportifs :
L'attention des sportifs sera attirée sur le fait que cette spécialité contient un principe actif pouvant induire une réaction positive des tests pratiqués lors des contrôles antidopage.
Nouveau-nés et prématurés :
Chez les nouveau-nés et les prématurés, l'utilisation prolongée du furosémide à forte posologie comportant un risque de néphrocalcinose et/ou lithiase intra-rénale, il est conseillé d'effectuer une surveillance échographique rénale.
INTERACTIONS |
Connectez-vous pour accéder à ce contenu
FERTILITÉ/GROSSESSE/ALLAITEMENT |
Grossesse
Les études effectuées chez l'animal ont mis en évidence un effet tératogène.
En clinique, il n'existe pas actuellement de données suffisamment pertinentes pour évaluer un éventuel effet malformatif du furosémide lorsqu'il est administré pendant la grossesse.
En règle générale, l'administration du furosémide doit être évitée chez la femme enceinte et ne jamais être prescrite au cours des œdèmes physiologiques (et ne nécessitant donc pas de traitement) de la grossesse.
Les diurétiques peuvent, en effet, entraîner une ischémie fœtoplacentaire, avec un risque d'hypotrophie fœtale.
Il convient de surveiller étroitement la croissance fœtale.
Les diurétiques (sous forme orale) restent néanmoins un élément essentiel du traitement des œdèmes d'origine cardiaque, hépatique et rénale survenant chez la femme enceinte.
Allaitement
Le furosémide est excrété dans le lait maternel. Le risque d'effets indésirables sur le nouveau-né ne peut être exclu. D'autre part, les diurétiques de l'anse diminuent la sécrétion lactée et la lactation est inhibée à partir d'une dose unique de 40 mg.
En conséquence, il est préférable de ne pas allaiter en cas de traitement par furosémide.
EFFETS INDÉSIRABLES |
Connectez-vous pour accéder à ce contenu
SURDOSAGE |
Une hypovolémie par déshydratation avec troubles électrolytiques peut être observée en cas de surdosage. Le traitement consiste en une compensation des pertes.
PHARMACODYNAMIE |
Connectez-vous pour accéder à ce contenu
PHARMACOCINÉTIQUE |
Connectez-vous pour accéder à ce contenu
DURÉE DE CONSERVATION |
Avant ouverture : 18 mois.
Après ouverture : 6 semaines au maximum.
PRÉCAUTIONS PARTICULIÈRES DE CONSERVATION |
A conserver à une température ne dépassant pas +30 °C.
Conserver le flacon dans l'emballage extérieur, à l'abri de la lumière.
Conserver le flacon soigneusement fermé, à l'abri de l'humidité.
PRÉCAUTIONS PARTICULIÈRES D'ÉLIMINATION ET DE MANIPULATION |
Ce médicament s'administre par voie orale, uniquement avec la pipette doseuse jointe au flacon de LASILIX 10 mg/ml, solution buvable.
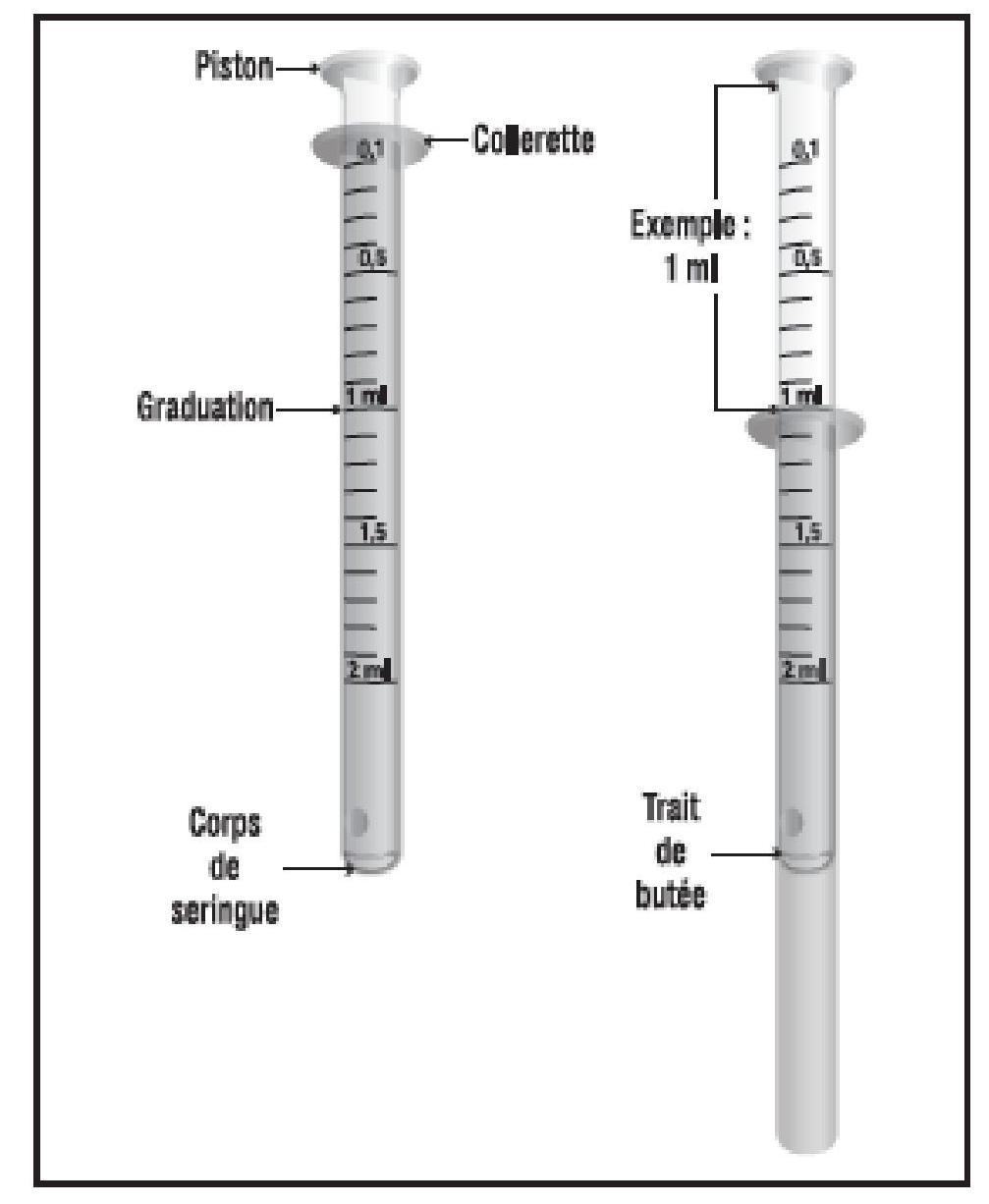
La dose à administrer pour une prise est obtenue en tirant le piston jusqu'à la graduation correspondant à la dose prescrite. La dose se lit au niveau de la collerette de la pipette doseuse pour administration orale.
Par exemple : pour prélever la dose à administrer de 1 ml, tirer le piston jusqu'à ce que la graduation 1 ml inscrite sur le piston atteigne la collerette de la pipette doseuse pour administration orale.
Après utilisation, refermer le flacon de la solution buvable, bien rincer la pipette doseuse pour administration orale avec de l'eau et sécher la pipette doseuse pour administration orale. Puis ranger immédiatement la pipette doseuse pour administration orale dans sa boîte dans un endroit inaccessible aux enfants. Ne jamais séparer la pipette doseuse pour administration orale des autres éléments de conditionnement du médicament (flacon, boîte, notice).
PRESCRIPTION/DÉLIVRANCE/PRISE EN CHARGE |
| AMM |
|
| Prix : |
|
