Le mogamulizumab est une immunoglobuline IgG1 de type kappa humanisée défucosylée qui se lie sélectivement au CCR4, un récepteur des chimiokines CC couplé à une protéine G, qui est impliqué dans la migration des lymphocytes vers différents organes, dont la peau, ce qui entraîne une déplétion des cellules cibles. Le récepteur CCR4 est exprimé à la surface de certaines cellules tumorales, y compris dans les néoplasies malignes à cellules T telles que le MF et le SS dans lesquels l'expression de CCR4 est inhérente.
Les fiches DCI Vidal constituent une base de connaissances pharmacologiques et thérapeutiques, proposée aux professionnels de santé, en complément des documents réglementaires publiés.
MOGAMULIZUMAB 4 mg/ml sol diluer p perf
Dernière modification : 27/11/2023 - Révision : 16/05/2022
| ATC | Risque sur la grossesse et l'allaitement | Dopant | Vigilance | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
L - ANTINEOPLASIQUES ET IMMUNOMODULATEURS L01 - ANTINEOPLASIQUES L01F - ANTICORPS MONOCLONAUX ET ANTICORPS-MEDICAMENTS CONJUGUES L01FX - AUTRES ANTICORPS MONOCLONAUX ET ANTICORPS-MEDICAMENTS CONJUGUÉS L01FX09 - MOGAMULIZUMAB |
| ||||||||||||||||||||||||||||||||||||||||||||
INDICATIONS ET MODALITÉS D'ADMINISTRATIONMOGAMULIZUMAB 4 mg/ml sol diluer p perfIndications
Ce médicament est indiqué dans les cas suivants :
- Mycosis fongoïde, traitement de 2e intention (du)
- Syndrome de Sézary, traitement de 2e intention (du)
PosologieUnité de priseml- mogamulizumab : 4 mg
Modalités d'administration- Voie intraveineuse (en perfusion)
- A diluer avant administration
- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
Posologie Patient à partir de 18 an(s) Patient quel que soit le poids Mycosis fongoïde, traitement de 2e intention (du) - Syndrome de Sézary, traitement de 2e intention (du) Traitement initial - Administrer une prémédication antihistaminique et antipyrétique
- Administrer à J1, J8, J15 et J22 du 1er cycle de 28 jours
- 1 mg/kg 1 fois par semaine
- Pendant 28 jours
Traitement ultérieur - Administrer à J1 et J15 de chaque cycle de 28 jours
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
- 1 mg/kg 1 fois ce jour toutes les 2 semaines
Modalités d'administration du traitement- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
- Réservé au sujet de plus de 18 ans
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
Incompatibilités physico-chimiques- Compatibilité avec certains matériaux
- Compatibilité avec certains solvants
- Incompatibilité avec tous les médicaments
Indications
Ce médicament est indiqué dans les cas suivants :
- Mycosis fongoïde, traitement de 2e intention (du)
- Syndrome de Sézary, traitement de 2e intention (du)
PosologieUnité de priseml- mogamulizumab : 4 mg
Modalités d'administration- Voie intraveineuse (en perfusion)
- A diluer avant administration
- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
Posologie Patient à partir de 18 an(s) Patient quel que soit le poids Mycosis fongoïde, traitement de 2e intention (du) - Syndrome de Sézary, traitement de 2e intention (du) Traitement initial - Administrer une prémédication antihistaminique et antipyrétique
- Administrer à J1, J8, J15 et J22 du 1er cycle de 28 jours
- 1 mg/kg 1 fois par semaine
- Pendant 28 jours
Traitement ultérieur - Administrer à J1 et J15 de chaque cycle de 28 jours
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
- 1 mg/kg 1 fois ce jour toutes les 2 semaines
Unité de priseml- mogamulizumab : 4 mg
Modalités d'administration- Voie intraveineuse (en perfusion)
- A diluer avant administration
- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
Posologie Patient à partir de 18 an(s) Patient quel que soit le poids Mycosis fongoïde, traitement de 2e intention (du) - Syndrome de Sézary, traitement de 2e intention (du) Traitement initial - Administrer une prémédication antihistaminique et antipyrétique
- Administrer à J1, J8, J15 et J22 du 1er cycle de 28 jours
- 1 mg/kg 1 fois par semaine
- Pendant 28 jours
Traitement ultérieur - Administrer à J1 et J15 de chaque cycle de 28 jours
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
- 1 mg/kg 1 fois ce jour toutes les 2 semaines
- Voie intraveineuse (en perfusion)
- A diluer avant administration
- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
Posologie Patient à partir de 18 an(s) Patient quel que soit le poids Mycosis fongoïde, traitement de 2e intention (du) - Syndrome de Sézary, traitement de 2e intention (du) Traitement initial - Administrer une prémédication antihistaminique et antipyrétique
- Administrer à J1, J8, J15 et J22 du 1er cycle de 28 jours
- 1 mg/kg 1 fois par semaine
- Pendant 28 jours
Traitement ultérieur - Administrer à J1 et J15 de chaque cycle de 28 jours
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
- 1 mg/kg 1 fois ce jour toutes les 2 semaines
- Administrer une prémédication antihistaminique et antipyrétique
- Administrer à J1, J8, J15 et J22 du 1er cycle de 28 jours
- 1 mg/kg 1 fois par semaine
- Pendant 28 jours
- Administrer à J1 et J15 de chaque cycle de 28 jours
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
- 1 mg/kg 1 fois ce jour toutes les 2 semaines
Modalités d'administration du traitement- Administrer par perfusion intraveineuse d'au moins 60 minutes
- En cas d'oubli : faire l'injection si oubli > 2 jours puis reprendre le rythme à cette date
- En cas d'oubli : si oubli < = 48 heures, faire l'injection dès que possible
- Ne pas agiter le flacon
- Réservé au sujet de plus de 18 ans
- Traitement à poursuivre jusqu'à la progression de la maladie ou la survenue de toxicité intolérable
Incompatibilités physico-chimiques- Compatibilité avec certains matériaux
- Compatibilité avec certains solvants
- Incompatibilité avec tous les médicaments
INFORMATIONS RELATIVES À LA SÉCURITÉ DU PATIENTMOGAMULIZUMAB 4 mg/ml sol diluer p perfNiveau de risque : X Critique III Haut II Modéré I Bas
Contre-indicationsX Critique Niveau de gravité : Contre-indication absolue - Hypersensibilité à l'un des composants
- Hypersensibilité aux protéines de hamster
PrécautionsII Modéré Niveau de gravité : Précautions- Charge tumorale importante
- Femme susceptible d'être enceinte
- Greffe de cellules souches hématopoïétiques
- Grossesse
- Hépatite B
- Hépatite B, antécédent
- Lymphome T cutané
- Présence d'anticorps anti-HBc
- Sujet à risque cardiaque
- Sujet de moins de 18 ans
- Tumeur à progression rapide
Interactions médicamenteusesSe référer au paragraphe Interactions médicamenteuses de la documentation officielle du produit
Grossesse et allaitement
Contre-indications et précautions d'emploi Grossesse (mois) Allaitement 1 2 3 4 5 6 7 8 9 Risques II II Précaution
Fertilité et Grossesse- Utiliser chez la femme une contraception efficace pdt le trt et au moins 6 mois après l'arrêt du trt
Risques liés au traitement- Risque d'infection sévère
- Risque de réaction cutanée sévère
- Risque de réaction d'hypersensibilité
- Risque de réaction liée à la perfusion
- Risque de réactivation virale
- Risque de syndrome de lyse tumorale
Surveillances du patient- Surveillance clinique pendant le traitement puis après l'arrêt du traitement
- Surveillance de l'ionogramme plasmatique en début de traitement
- Surveillance de la fonction rénale en début de traitement
- Surveillance dermatologique pendant le traitement
- Surveillance médicale avec disponibilité de matériel de réanimation pendant le traitement
- Surveillance par un test de dépistage d'une infection par le virus de l'hépatite B avant le trt
Mesures à associer au traitement- A diluer avant administration
- Administrer une prémédication antihistaminique et antipyrétique
- Traçabilité recommandée
Traitement à arrêter définitivement en cas de...- Traitement à arrêter en cas d'apparition de réaction d'hypersensibilité
- Traitement à arrêter en cas de réaction cutanée sévère
- Traitement à arrêter en cas de réaction liée à la perfusion engageant le pronostic vital
Effets indésirables
Systèmes Fréquence de moyenne à élevée (?1/1 000) Fréquence basse (<1/1 000) Fréquence inconnue ANOMALIE DES EXAMENS DE LABORATOIRE Lymphopénie (Fréquent)
ASAT (augmentation) (Fréquent)
Neutropénie (Fréquent)
Leucopénie (Fréquent)
Phosphatases alcalines (augmentation) (Fréquent)
ALAT (augmentation) (Fréquent)
Anticorps spécifique à la substance
CANCEROLOGIE Syndrome de lyse tumorale (Peu fréquent)
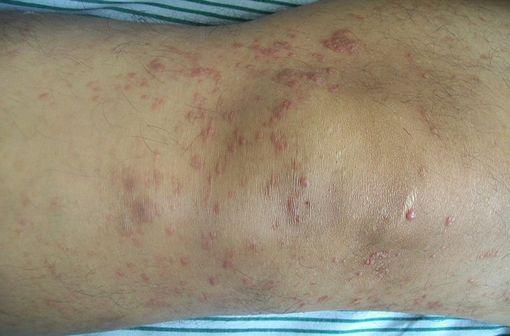
DERMATOLOGIE Eruption d'origine médicamenteuse (Très fréquent)
Eruption cutanée
Cellulite
Réaction cutanée
Folliculite
Infection cutanée
DIVERS Fatigue (Très fréquent)
Fièvre (Très fréquent)
Oedème périphérique (Très fréquent)
ENDOCRINOLOGIE Hypothyroïdie (Fréquent)
HÉMATOLOGIE Thrombopénie (Fréquent)
Anémie (Fréquent)
HÉPATOLOGIE Hépatite aiguë (Peu fréquent)
Hépatite (Peu fréquent)
IMMUNO-ALLERGOLOGIE Déficit immunitaire
INFECTIOLOGIE D'ORIGINE BACTERIENNE Infection staphylococcique
INFECTIOLOGIE D'ORIGINE FONGIQUE Candidose
INFECTIOLOGIE D'ORIGINE VIRALE Herpès
Infection à cytomégalovirus
Zona
INFECTIOLOGIE NON PRECISÉE Infection (Très fréquent)
Sepsis
INSTRUMENTATION Réaction liée à la perfusion (Très fréquent)
ORL, STOMATOLOGIE Stomatite (Très fréquent)
Otite externe
SYSTÈME DIGESTIF Nausée (Très fréquent)
Constipation (Très fréquent)
Diarrhée (Très fréquent)
Vomissement (Fréquent)
SYSTÈME MUSCULO-SQUELETTIQUE Polymyosite
SYSTÈME NERVEUX Céphalée (Très fréquent)
SYSTÈME RESPIRATOIRE Infection des voies respiratoires supérieures (Fréquent)
Insuffisance respiratoire
Pneumonie
UROLOGIE, NÉPHROLOGIE Infection urinaire
| Niveau de risque : | X Critique | III Haut | II Modéré | I Bas |
|---|
Contre-indicationsX Critique Niveau de gravité : Contre-indication absolue - Hypersensibilité à l'un des composants
- Hypersensibilité aux protéines de hamster
Niveau de gravité : Contre-indication absolue - Hypersensibilité à l'un des composants
- Hypersensibilité aux protéines de hamster
|
PrécautionsII Modéré Niveau de gravité : Précautions- Charge tumorale importante
- Femme susceptible d'être enceinte
- Greffe de cellules souches hématopoïétiques
- Grossesse
- Hépatite B
- Hépatite B, antécédent
- Lymphome T cutané
- Présence d'anticorps anti-HBc
- Sujet à risque cardiaque
- Sujet de moins de 18 ans
- Tumeur à progression rapide
Niveau de gravité : Précautions- Charge tumorale importante
- Femme susceptible d'être enceinte
- Greffe de cellules souches hématopoïétiques
- Grossesse
- Hépatite B
- Hépatite B, antécédent
- Lymphome T cutané
- Présence d'anticorps anti-HBc
- Sujet à risque cardiaque
- Sujet de moins de 18 ans
- Tumeur à progression rapide
|
Interactions médicamenteusesSe référer au paragraphe Interactions médicamenteuses de la documentation officielle du produit
Grossesse et allaitement
| Contre-indications et précautions d'emploi | ||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||
Fertilité et Grossesse- Utiliser chez la femme une contraception efficace pdt le trt et au moins 6 mois après l'arrêt du trt
Risques liés au traitement- Risque d'infection sévère
- Risque de réaction cutanée sévère
- Risque de réaction d'hypersensibilité
- Risque de réaction liée à la perfusion
- Risque de réactivation virale
- Risque de syndrome de lyse tumorale
Surveillances du patient- Surveillance clinique pendant le traitement puis après l'arrêt du traitement
- Surveillance de l'ionogramme plasmatique en début de traitement
- Surveillance de la fonction rénale en début de traitement
- Surveillance dermatologique pendant le traitement
- Surveillance médicale avec disponibilité de matériel de réanimation pendant le traitement
- Surveillance par un test de dépistage d'une infection par le virus de l'hépatite B avant le trt
Mesures à associer au traitement- A diluer avant administration
- Administrer une prémédication antihistaminique et antipyrétique
- Traçabilité recommandée
Traitement à arrêter définitivement en cas de...- Traitement à arrêter en cas d'apparition de réaction d'hypersensibilité
- Traitement à arrêter en cas de réaction cutanée sévère
- Traitement à arrêter en cas de réaction liée à la perfusion engageant le pronostic vital
Effets indésirables
| Systèmes | Fréquence de moyenne à élevée (?1/1 000) | Fréquence basse (<1/1 000) | Fréquence inconnue |
|---|---|---|---|
| ANOMALIE DES EXAMENS DE LABORATOIRE | |||
| CANCEROLOGIE | |||
| DERMATOLOGIE | |||
| DIVERS | |||
| ENDOCRINOLOGIE | |||
| HÉMATOLOGIE | |||
| HÉPATOLOGIE | |||
| IMMUNO-ALLERGOLOGIE | |||
| INFECTIOLOGIE D'ORIGINE BACTERIENNE | |||
| INFECTIOLOGIE D'ORIGINE FONGIQUE | |||
| INFECTIOLOGIE D'ORIGINE VIRALE | |||
| INFECTIOLOGIE NON PRECISÉE | |||
| INSTRUMENTATION | |||
| ORL, STOMATOLOGIE | |||
| SYSTÈME DIGESTIF | |||
| SYSTÈME MUSCULO-SQUELETTIQUE | |||
| SYSTÈME NERVEUX | |||
| SYSTÈME RESPIRATOIRE | |||
| UROLOGIE, NÉPHROLOGIE |
Voir aussi les substances
Mogamulizumab
Chimie
| IUPAC | immunoglobuline G1-kappa, anti-[Homo sapiens CCR4 (récepteur 4 de chimiokine (C-C motif), récepteur 4 de chimiokine CC, CCR-4, CKR4, k5-5, CD194)], anticorps monoclonal humanisé; chaîne lourde gamma1 (1-449) [VH humanisé (Homo sapiens IGHV3-21*01 (83.70%) -(IGHD)-IGHJ4*01) [8.8.12] (1-119) -Homo sapiens IGHG1*01 (120-449)], (222-219')-disulfure avec la chaîne légère kappa (1'-219') [V-KAPPA humanisé (Homo sapiens IGKV2- 29*02 (81.00%) -IGKJ1*01) [11.3.9] (1'-112') -Homo sapiens IGKC*01 (113'-219')]; dimère (228-228":231-231")-bisdisulfure |
|---|---|
| Synonymes | mogamulizumab |